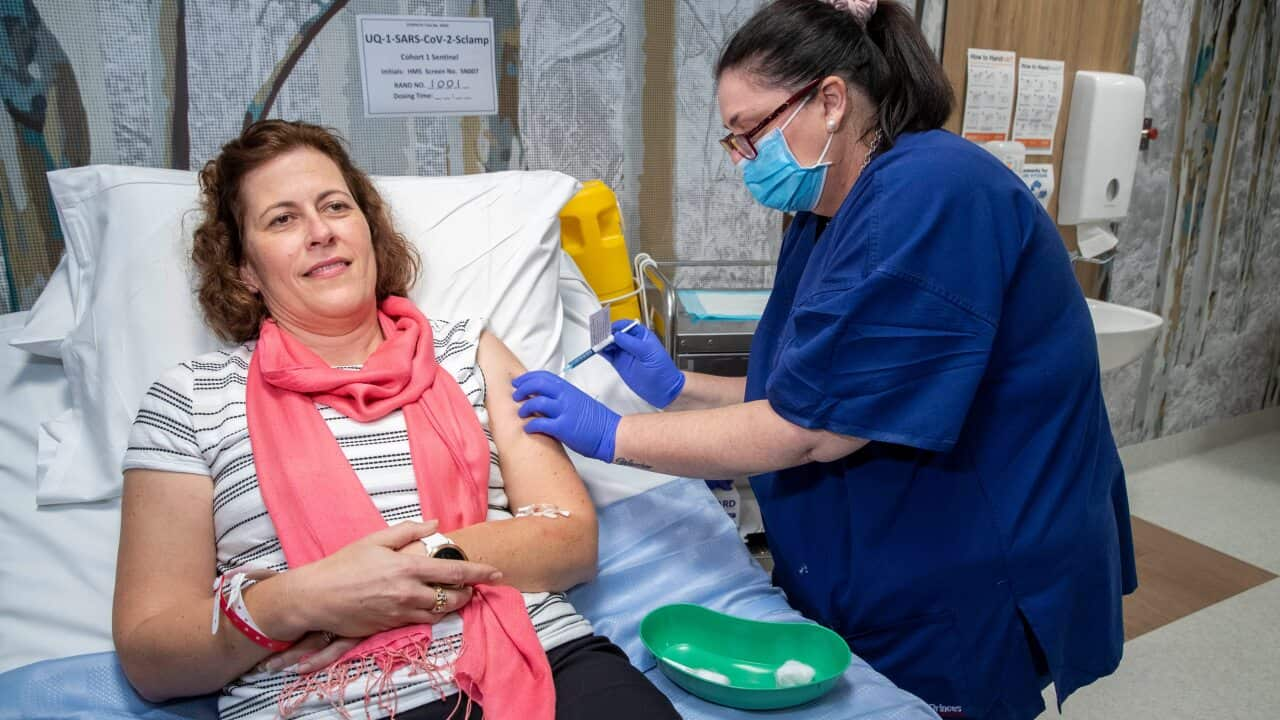
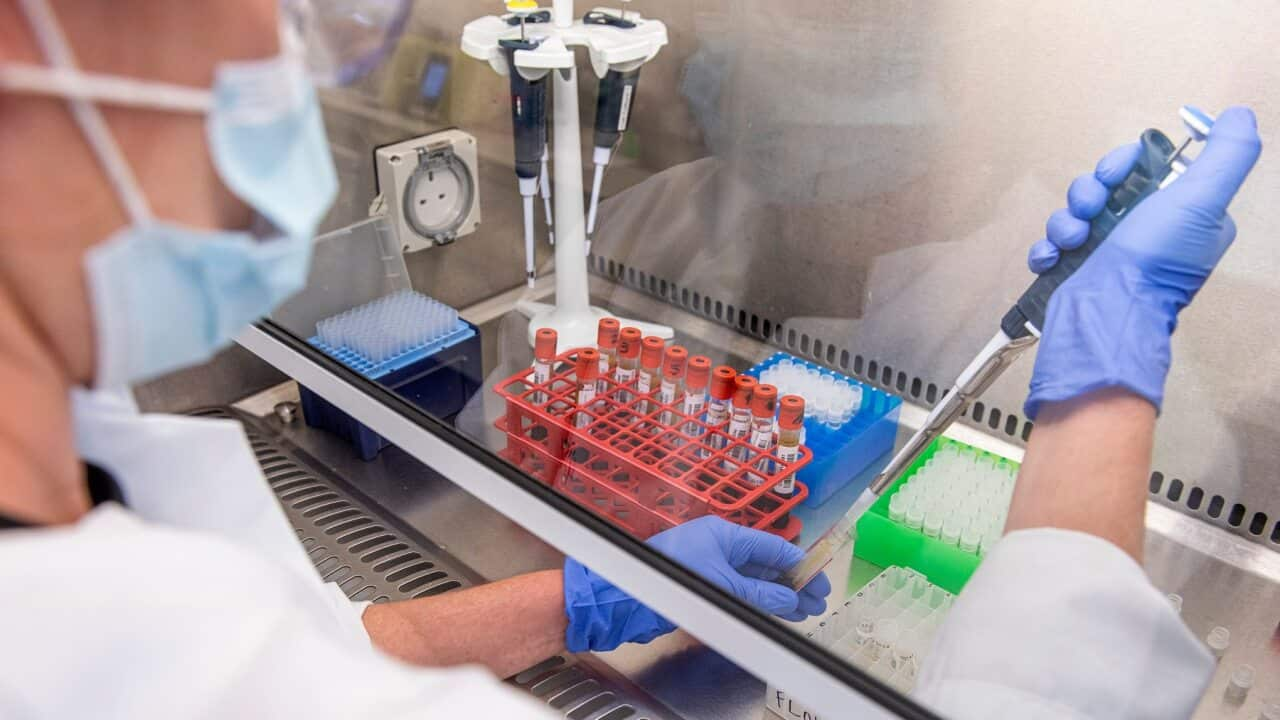
牛津大学COVID-19疫苗人体试验的一名参与者出现严重不良反应,目前该疫苗的试验被暂停。
此前,澳大利亚政府称已达成意向,只要该疫苗试验成功,明年初澳大利亚人就能接种。
联邦副首席医学官尼克·科茨沃思(Nick Coatsworth)说,试验延期并不一定意味着疫苗协议已经无效,但不良反应有待调查。
他并不担心试验被暂停,并赞扬了疫苗试验的透明度。
他周三告诉九号台:“我将等着看到底是什么不良反应,以及这是否将其归因于疫苗。”
阿斯利康公司(AstraZeneca)证实,一名英国参与者出现不明病症,该试验已被自愿暂停。
一个独立的委员会现在将着手审查数据。
阿斯利康在一份声明中说:“这是一项常规行动,每当在试验中出现不明原因的疾病时,就必须进行调查,以确保我们保持试验的完整性。”
“在大型试验中,疾病会偶然发生,但必须进行独立审查,仔细检查这一点。”
“我们正努力加快对单个事件的审查,以最大限度地减少对试验时间表的潜在影响。我们致力于参与者的安全和试验的最高行为标准。”
阿斯利康(AstraZeneca)的一位发言人证实,暂停了在美国和其他国家进行的疫苗研究。
8月下旬,阿斯利康开始在美国招募3万名参与者,进行其最大规模的疫苗研究。
它在英国针对数千人测试这款由牛津大学开发的疫苗,在巴西和南非也进行了小规模的研究。
另外两种疫苗正在美国进行最后阶段的大规模测试,一种由莫德纳(Moderna)公司生产,另一种由辉瑞和德国的BioNTech公司生产。
这两种疫苗的原理与阿斯利康不同,而且这些研究已经招募了大约三分之二的志愿者。
大型医学研究临时暂停并不罕见,调查任何严重或意外的反应是安全测试的强制性部分。
就在这一事态发展的同一天,阿斯利康和其他八家制药商发表了一项不同寻常的承诺,誓言在开发疫苗时坚持最高的伦理和科学标准。
该声明发布之前,有人担心美国总统特朗普(Donald Trump)将向美国食品药品监督管理局(FDA)施加压力,要求其在证明安全有效之前批准疫苗。
美国已投入数十亿元,以快速开发针对COVID-19的多种疫苗。
但公众担心,疫苗不安全或无效可能造成灾难性后果。
READ MORE

如何订阅SBS中文的newsletter?
澳大利亚人必须与他人保持至少1.5米的社交距离,请查看您所在州或领地的最新社交限制措施。
如果您出现感冒或流感症状,请留在家中并致电家庭医生或全国冠状病毒健康信息热线1800 020 080安排测试。
SBS致力于用63种语言报道最新的COVID-19新闻和信息,详情请前往:sbs.com.au/coronavirus。
READ MORE

澳大利亚各州和领地实施的COVID-19限制措施
READ MORE

澳洲COVID-19新冠疫情和疫苗:我们必须了解的信息