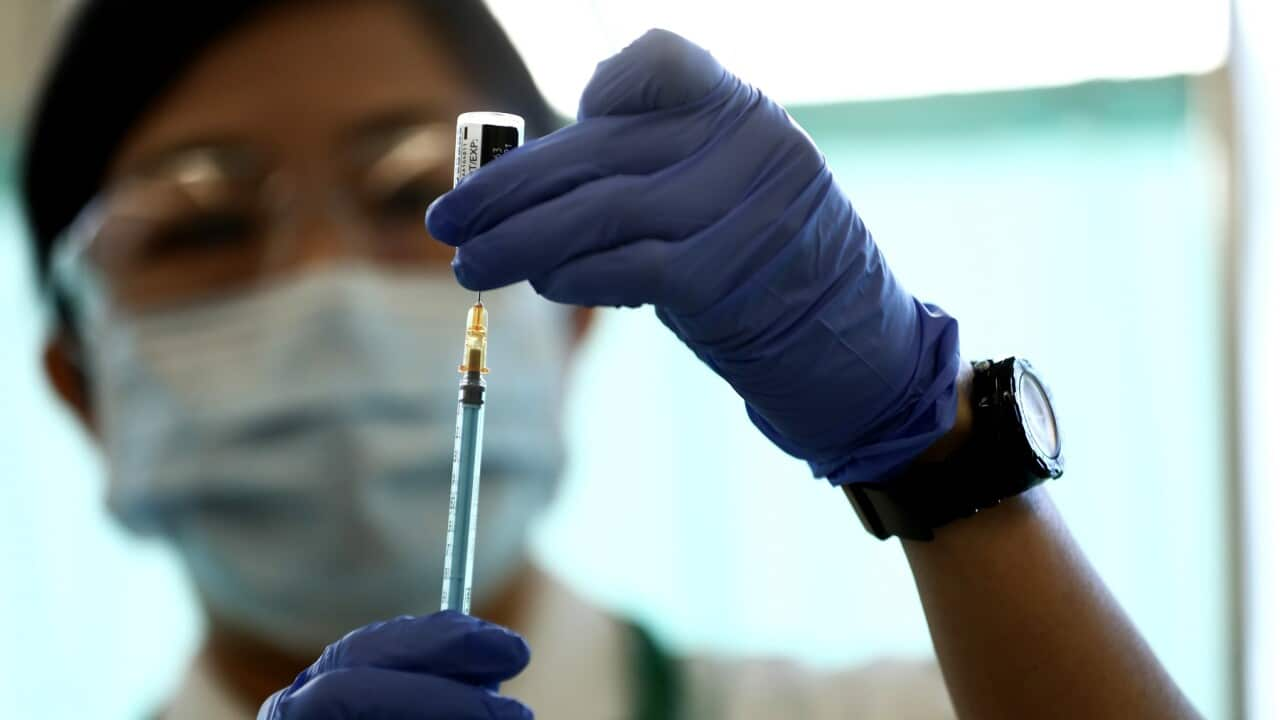
澳大利亚的首批新冠疫苗接种已经从上周日起拉开帷幕。已经近在身边的疫苗一方面让人们看到了疫情结束的曙光,另一方面也让一部分人心存疑虑。尤其一般疫苗从研发到推出市场需时十年,但新冠疫苗却在一年内就面世,让不少朋友想要知道:疫苗研发这么快,安全有保证吗?
冯高谦博士是墨尔本伯内特医学研究院的免疫学专家。他在接受SBS中文采访时,分析了新冠疫苗如此快速问世的三大原因。
1. 政府和企业的巨额投入
百年一遇的疫情使得各国政府和医药企业高度重视新冠危机,巨额的资金和资源投入以及各方的政策支持令一些可能导致研发拖延的因素被很快克服。
比如多项临床试验得以迅速启动,制药公司可以不惜代价,在知道疫苗是否有效前就生产和储存疫苗。
2 疫苗研发并不是“从零开始”
参加新冠疫苗研发的一些大型制药公司,在本次疫情爆发之前就有了成熟的疫苗平台。 冯高谦博士以澳洲首批接种的辉瑞/BioNTech的新冠疫苗为例指出,这种mRNA疫苗早在新冠爆发之前就已经用于某些癌症的防治,载体早已研发成功。本次新冠疫苗的研发团队只是改换了载体上的抗原mRNA,将它换成中国科学家早在2020年就公布的新冠病毒基因序列。
冯高谦博士以澳洲首批接种的辉瑞/BioNTech的新冠疫苗为例指出,这种mRNA疫苗早在新冠爆发之前就已经用于某些癌症的防治,载体早已研发成功。本次新冠疫苗的研发团队只是改换了载体上的抗原mRNA,将它换成中国科学家早在2020年就公布的新冠病毒基因序列。

新冠疫苗生產商、美國生物技術公司莫德納(Moderna)的科學家表示,其研製的新冠疫苗似乎可以對抗現時在英國和南非發現的變種新冠病毒。 Source: Getty Images
已经有了一个非常成熟的平台,又有了这个病毒的这些相关信息,再去研发一个新冠疫苗的话,相对来讲其实不是一个很难的事。
本次爆发疫情的元凶——新冠病毒隶属冠状病毒家族。这让人们可以基于其同类病毒SARS(严重急性呼吸道综合征)和MERS (中东呼吸综合症)的研究更进一步获得认识,并应用已经成熟的相关技术。
3 疫情的广泛为临床试验节省了时间
一种疫苗从实验室研发到大规模接种,需要经过三轮人体临床试验。
- 第一阶段:在几十人到一两百人身上进行测试,这部分旨在确保疫苗是安全的。
- 第二阶段:更多的人体试验——几百人到一两千人,平衡疫苗安全和有效的两项属性。
- 第三阶段:进行大量人体试验,确认其有效性和安全性。
冯高谦博士说,一般临床试验是疫苗推出之前最耗时的环节。但由于疫情在欧洲、北美和南美的大规模爆发,再加上大量的资金注入,研究人员招募参与研究的人难度大大降低,在临床试验中“形成统计学差异”成了一件容易的事,因而给快速研发疫苗又不牺牲其安全性带来了可能。
即使在疫苗已经获得批准和许可,仍然面临所谓的第四阶段临床试验——也就是在疫苗上市以后对其疗效和不良反应的长期追踪。在澳大利亚,与接种疫苗有关的不良事件会直接汇报给卫生和民政部(Department of Human Services and Health)。监管机构会继续参与其中,监督疫苗生产,检查制造设施,继续监测产品的安全性和有效性。
点击封面图片收听吴音对墨尔本伯内特医学研究院冯高谦博士的完整采访,权威解答您想了解的疫苗问题。
READ MORE

你好,澳大利亚
澳大利亚人必须与他人保持至少1.5米的社交距离,请查看您所在州或领地的最新社交限制措施。
如果您出现感冒或流感症状,请留在家中并致电家庭医生或全国冠状病毒健康信息热线1800 020 080安排测试。
SBS致力于用63种语言报道最新的COVID-19新闻和信息,详情请前往:sbs.com.au/coronavirus。